摘要
目的:在回顾性单中心研究中,评价以GnRHa类似物治疗对特发性中枢性性早熟(idiopathic central precocious puberty,ICPP)女孩成年身高(AH)、体重指数(BMI)、骨矿物质密度(BMD)和生殖功能的影响。
病人:87名ICPP病人以GnRHa治疗4.2±1.6年(范围3–7.9年),在停止治疗后观察9.9±2.0岁(范围4–10.6岁)。为了更好地评价效果,也研究了32名未治疗的类似ICPP 病人。
结果:成年身高为159.8±5.3cm,显著高于Bayley和Pinneau发育提前和一般表预测的成年身高(PAH),治疗前PAH与AH之间的身高增加分别为5.1±4.5和9.5±4.6cm。治疗期间的激素数值和卵巢、子宫直径下降;停止治疗1年后增加到正常。在停止治疗后0.9±0.4年出现初潮,平均年龄为13.6±1.1岁,月经正常。有6名女孩怀孕,并正常分娩了后代。在治疗前、中、后,生活年龄BMI增长,但无统计学显著性。在停止治疗时的BMD下降,在性腺活动正常时增加到对照值。
结论:以GnRHa治疗ICPP,对于生殖系统、BMD和BMI是安全的,有助于使成年身高接近靶身高;但是个体反应的可变性提示,应选择除身高增长以外更多的参数,特别是对8岁以上开始青春期发身的女孩。
J Clin Endocrinol Metab, 2008, 93(1):190-195.
前言
使用GnRH类似物(GnRHa)治疗中枢性性早熟(central precocious puberty, CPP)已有20多年的历史了。虽然以GnRHa治疗多年的许多CPP受试者已经达到了成年身高,但成年身高(AH)的改善仍然存在争议。已有许多CPP病人大样本治疗中和停止治疗后的长期观察以及跟踪研究。在本单一中心的回顾性研究中, 对87名以GnRHa治疗的特发性中枢性性早熟(idiopathic central precocious puberty, ICPP) 病人停止治疗后数年内进行了观察,评价对AH、BMI、BMD和生殖功能的影响。
受试者和方法
受试者
87名以GnRHa治疗4.2±1.6年(范围3–7.9年)的ICPP女孩,在停止治疗后观察了9.9±2.0年(范围4–10.6年),表1和表2.
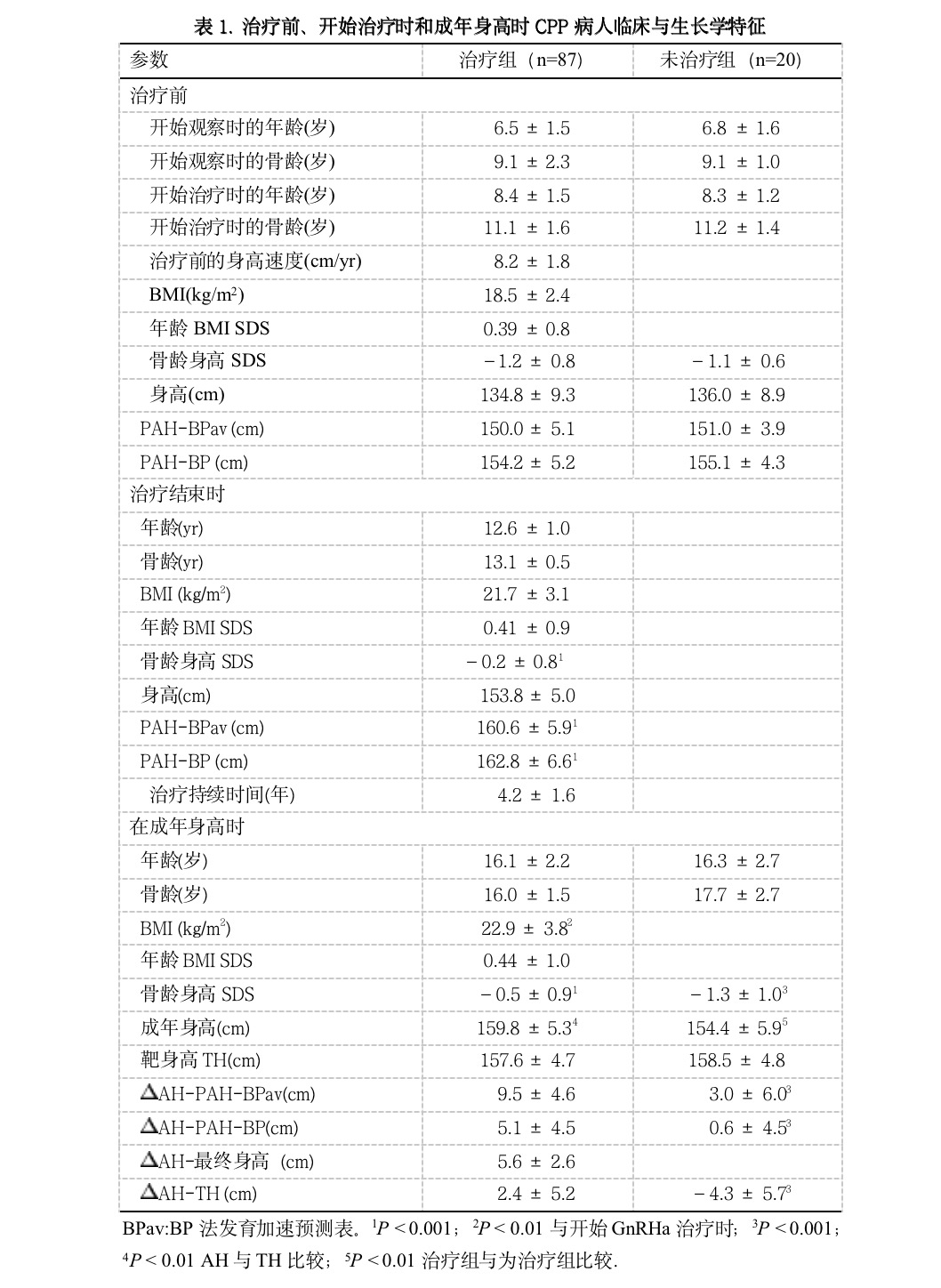
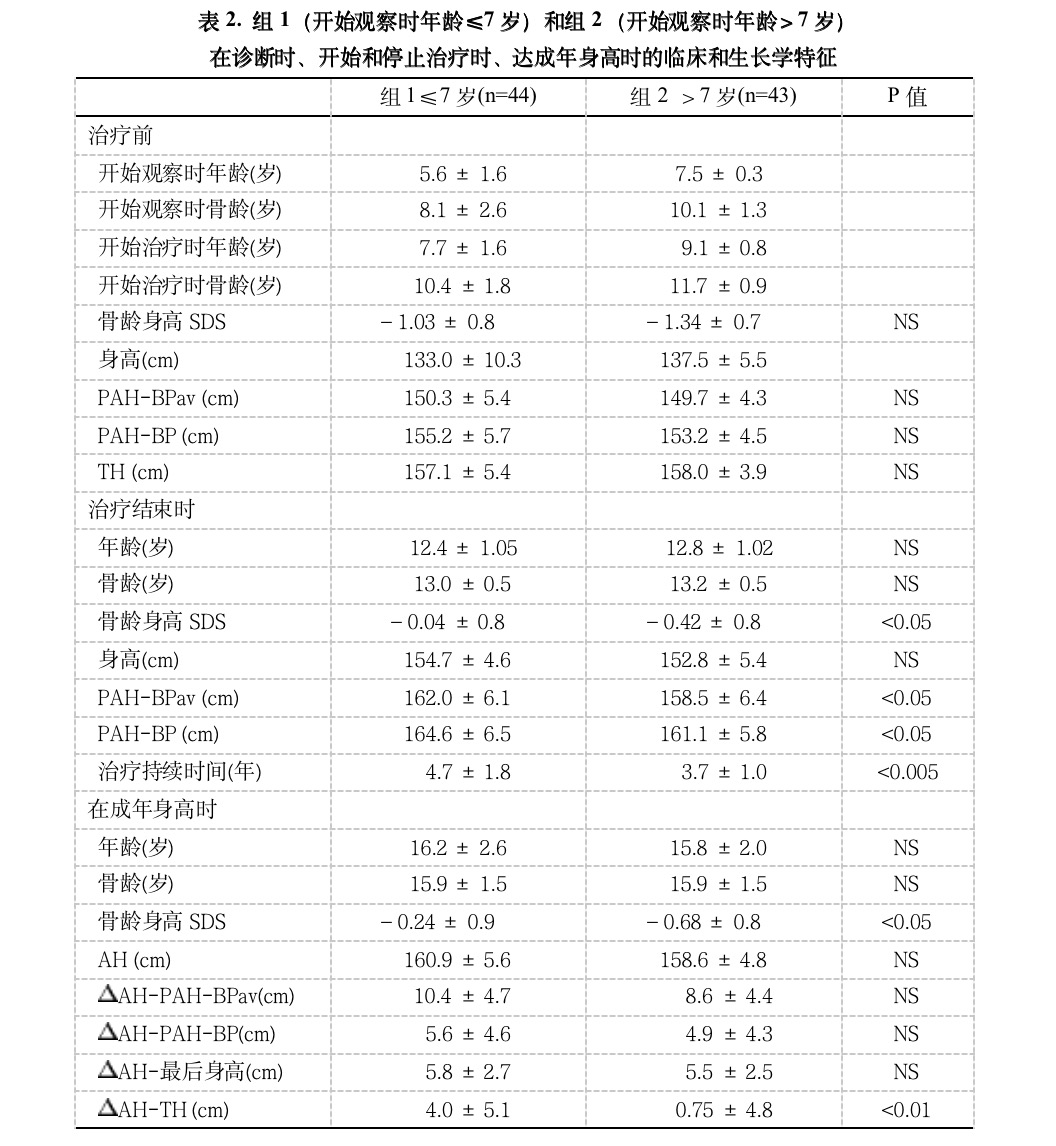
根据下列典型标准诊断CPP:1)在生活年龄(CA)8岁前乳房开始发育(Tanner等级B2或以上);2)对GnRHa刺激试验出现青春期LH反应(>7 IU/l);3)身高速度增加和骨龄(BA)提前生活年龄至少1岁;4)子宫超声长度大于3.5cm和卵巢体积大于1.5cm3。磁共振成像(MRI)无下丘脑-垂体器质性病变表现,我们将这些女孩分类为特发性CPP。在追踪的数年中,重复MRI证实了最初的诊断结果。在年龄最小的以及临床表现有特别发展的受试者,我们重复了MRI检查,检查数量和次数不定。从第一次观察开始评价个人病史、青春期发身速度及其所发生的心理学问题。开始评价时的CA为6.5±1.5岁(范围1.2–7.9岁), BA为9.1±2.3岁 (范围2–11岁)。虽然在最初评价时的CA一般大于发身症状出现时的CA,但我们决定不以发身开始年龄,而是以最初观察年龄进行统计分析。最初的评价包括测量身高、发身等级、BA、基础血浆雌二醇水平、对GnRHa刺激试验的LH和FSH反应。对于阴毛出现为最初发身征兆和骨龄显著提前的女孩,进行静脉ACTH试验,测量基础的和刺激后的17α-羟孕酮和睾酮水平,以排除非典型的先天性肾上腺增生共存疾病的可能性。在至少6个月的观察期,排除暂时或缓慢进展形式的CPP后,进行GnRHa治疗。病人以每21-25天肌肉注射100-120ug/kg剂量的长效曲普瑞林(D-TRP6-LHRH)治疗。在第一次注射GnRHa前、后21天,口服100mg/d的醋酸环孕酮(分两次口服),以预防突发升高期促性腺激素的刺激作用,最后一周剂量减小到50mg/d。开始治疗时的CA为8.4±1.5岁(范围1.7–9.5岁), BA为11.1±1.6岁 (范围3–12岁)。在治疗期间,每6个月评价一次身高、体重、BA、发身等级和标准GnRH试验后的LH与FSH,以估价垂体-性腺轴的抑制情况。调整GnRHa剂量以保持垂体-性腺轴的完全抑制,以GnRH实验和其后治疗中的体重变化来证实。在女孩CA为12.6±1.0 岁(范围10.2–13.5岁)和BA为13.1±0.5岁(范围12–14.2岁)时停止治疗。在停止治疗后的观察期内,所有女孩达到了成年身高(AH)。当前1年身高生长不足1cm,BA在15岁以上时确定为达到了成年身高。计算每名病人治疗前、中、后的BMI,以检验显著的变化。在停止治疗时及其后每年评价BMD。
对于生殖功能,评价治疗过程中每6个月的FSH和LH水平和子宫超声长度、卵巢体积。停止治疗后,评价初潮的恢复、月经后期、怀孕的能力及胎儿的出生。
为了更好地评价治疗效果,我们分析32名与治疗组相似的同代未治疗女孩。这些女孩因不同的原因拒绝GnRHa治疗,但继续在观察之中。
方法
在每次评价时,由同一名观察者使用Harpenden测距仪测量3次身高;使用Marshall和Tanner标准评价发身等级;由两名观察者根据Greulich和Pyle图谱评价骨龄;使用Bayley和Pinneau法对每名病人预测两次成年身高:骨龄提前生活年龄1岁及以上使用加速女孩表(PAH-BP),对于骨龄与CA在1岁以内的女孩使用一般女孩表(PAH-BPav),也与Kauli et al.所提示的一样,无论骨龄提前多少,对所有病人也都使用一般女孩表预测成年身高。以性别调整的父母身高中值计算靶身高(TH)。以体重除以身高的平方计算BMI,并以年龄SDS表示以双能X线吸收法在L2-L4水平上测量腰椎整块骨(皮质骨和小梁骨)的BMD,其数值使用扫描的椎骨面积修正,表示为BMD(g/cm2)。使用双能X线吸收法得出的数据计算腰椎体积BMD(vBMD),以g/cm3表示,将椎体作为椭圆柱体,由侧面扫描的骨矿物质含量(g)除以椎体体积(m3 ,计算方法= p×宽/2× 深/2 ×高),以减小骨体积的混淆影响。
统计分析
以平均数和标准差表示数据。使用t检验评估统计分析结果。使用pearson相关系数确定两参数之间的关系。P<0.05为显著性水平。
结果
在第一次观察时,平均CA和BA分别为6.5±1.5岁和9.1±2.3岁;在开始治疗时CA、BA、身高和BMI分别为8.4±1.5岁、11.1±1.6岁、134.8±9.3 cm和18.5±2.4 kg/m2;在GnRHa治疗4.2±1.6年达到的成年身高为159.8 5.3cm。因为治疗前的PAH为154.2±5.3cm(发育加速表)和150.1±5.1cm (BP发育一般表),所以治疗对AH的增加分别为5.1±4.5cm和9.5±4.6cm。AH高于TH(P < 0.01)。AH与几个参数之间的回归分析表明(表3),与TH、治疗开始和治疗结束身高、治疗开始前后身高的PAH正相关,与治疗持续时间无相关,与其它作者的研究相一致。
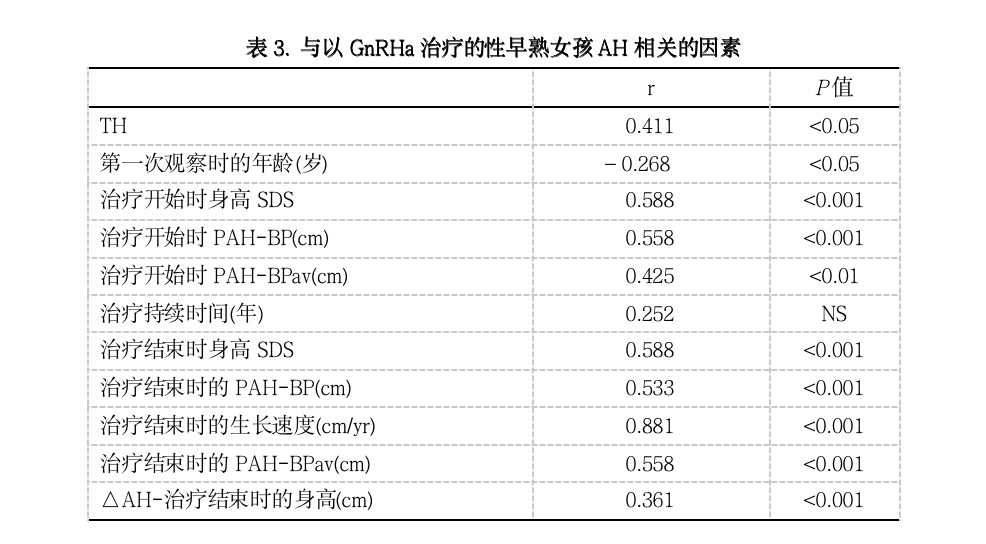
为研究生长结果是否会受到青春期开始年龄的影响,我们将受试者分为两组:组1的CA小于7岁(n=44),组2的CA大于7岁(n=43),发现两组的AH和相对于预测成年身高增加的差异无显著性(表2)。87名治疗女孩与32名类似未治疗的对照组女孩的比较表明,未治疗女孩的AH与治疗女孩相比显著较低(5.4 cm)、也显著低于TH(4.3±5.7cm;P < 0.01)和PAH(一般预测表约低6cm;加速预测表约低5cm,P<0.001,表1)。因为儿童的BMI与年龄有关,所以既以全组,也以7岁前后开始的两组进行分析,观察到治疗过程中的显著增长。但是在治疗开始时,年龄BMI SDS为0.39±0.8,在治疗结束时0.41±0.9,几年后为0.44±1.0,未发现显著性差异,并非所有病人超重或肥胖(开始治疗时分别为14.3和9.1%;在治疗结束时和几年后的成年身高时都为11.7%)。除个别数据外,我们观察到,虽然在治疗全过程中BMI百分位数或SDS保持不变,但BMI基本上是增长的。而且,在治疗结束时超重或肥胖的病人处于开始时的相同位置上。回归分析表明,治疗结束时与开始治疗时的生活年龄BMI SDS正相关(P < 0.001;r = 0.332)。
在87名病人中有67名评价了BMD。在治疗结束时,平均BMD和vBMD分别为0.82±0.01 g/cm2 和0.135±0.03 g/cm3,二者均显著低于对照组(1.001± 0.11 g/cm2和0.143±0.03 g/cm3, P < 0.001)。在性腺活动完全恢复后,平均BMD增加到1.000±0.11g/cm2,与对照组(1.015±0.11g/cm2)无显著性差异;同样vBMD增加到0.165±0.01g/cm3,与对照组(0.166±0.02g/cm3)也无显著性差异。治疗过程中的LHRH试验后血浆FSH和LH受到抑制,显著低于治疗前(LH峰为0.6±0.7对24.2±28.3IU/l;FSH峰位 1.6±1.0对13.2±7.1 IU/l, 二者 P < 0.005)。在治疗后1年时,LH峰和FSH峰分别回升到30.3±16.0和11.5±11.9 IU/l(P < 0.005)。治疗过程中雌二醇水平(8 ± 2.8 pg/ml)显著低于治疗前(26.9±5.5 pg/ml;P < 0.001),在治疗停止后1年上升到64.9±13.6 pg/ml(P < 0.001)。卵巢体积由2.8±1.3cm3下降到治疗中的1.9±1.0cm3,增加到5.4±3.2 cm3 (P < 0.001);治疗过程中子宫长度无变化(4.6±0.8 cm)治疗后1年时增加到6.7±0.9 cm (P < 0.001)。在平均年龄13.6±1.1岁时(停止GnRHa治疗后0.9±0.4年)出现月经初潮。月经史表明,82名病人有规律的月经周期,其余5名因高强度的运动而月经稀发,在降低运动强度后的2-3年内问题得以解决。6名女孩怀孕并正常分娩了后代(图1和图2)。
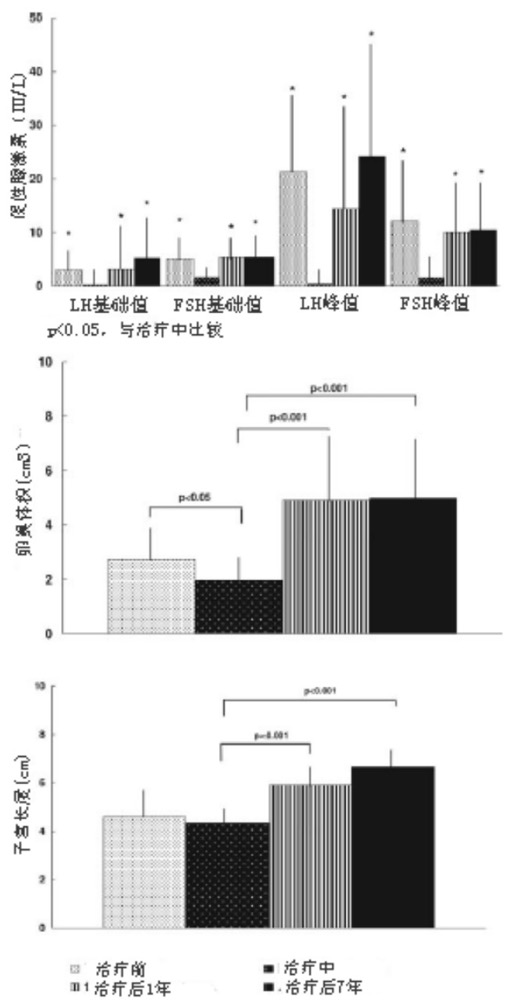
图1. ICPP女孩LH和FSH基础水平和GnRH刺激试验后水平;
治疗前、中、后1年和7年时卵巢体积与子宫纵向长度
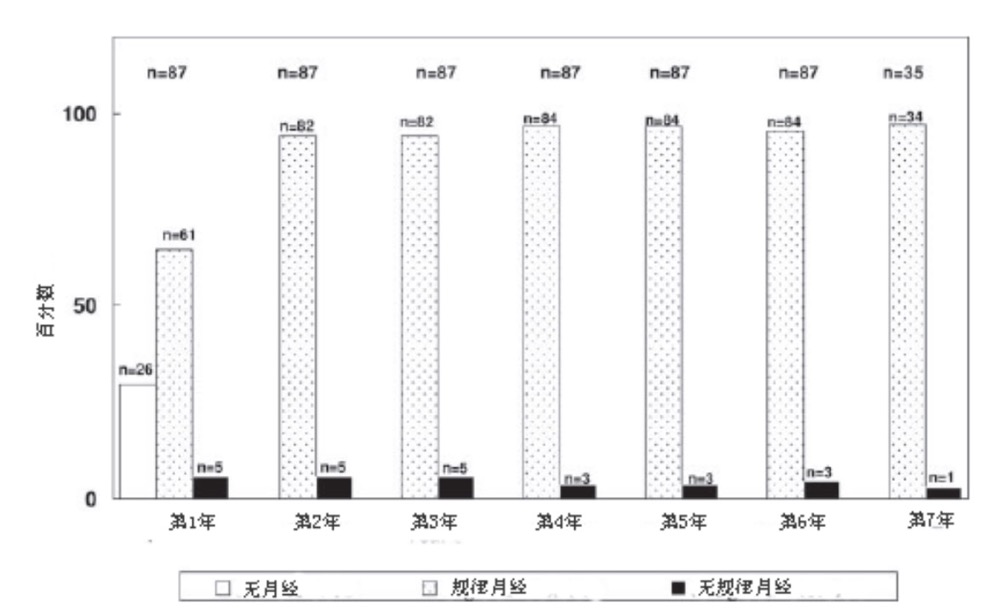
图2. ICPP女孩治疗后1,2,3,4,5,6,7年时的月经表现
讨论ICPP是6-8岁CPP女孩最常见的病因。因为这些病人代表了相对同类的人群,所以可比器质性CPP更准确地评价使用GnRHa治疗对成年身高的影响。作为整体,87名病人的AH达到或超过了TH,显著高于治疗前的PAH。与治疗组相比,未治疗组女孩所达到的AH低5cm左右,也比她们的TH低4cm,与一般预测表的PAH相比增加无显著性,与发育提前预测表的PAH相比无增加。我们的结果证实,在7岁前与7岁后开始发身女孩之间,AH减治疗前PAH的身高增加差异无显著性。根据意大利仍然使用8岁作为诊断性早熟界值年龄的情况来看,可以7岁上下分组。当然,在5-6岁以下的儿童治疗效果更显著,其身高潜力可恢复到TH范围内。所观察到这些病人对GnRHa生长反应的极端可变性提示,在决定是否应当治疗时,应当考虑除生长学以外的其它因素。治疗中和治疗后的BMI的形式仍然是存有争议的问题。某些作者报告自始至终显著增长,有的作者甚至报告了治疗开始阶段BMI下降。与其它研究报告相比,我们样本中的超重和肥胖者数量较少,我们观察到,除了个别数据外,BMI总体上是增长的,尽管仍然处于相同的百分位数或SDS位置上。而且,在治疗结束时超重和肥胖病人所处的位置与治疗开始时相同。总之,GnRHa未导致显著地BMI增长。以前研究证明卵巢活动抑制是开始治疗1年后BMD下降的原因。我们观察到停止治疗几年后达到AH时,卵巢活动完全得以恢复,矿物质含量完全恢复,达到骨量峰值。得出结论为,治疗过程中GnRHa抑制了矿物质含量的获取,但治疗后矿物质含量恢复。未观察到有关的副作用(皮疹、过敏反应)。由促性腺激素和雌二醇水平或子宫长度和卵巢的完全发育,提示所有病人的下丘脑-垂体-性腺轴再活化。与其他作者的观察一样,在治疗结束后1年左右出现初潮,并有规律的月经周期,6名女孩怀孕正常分娩了后代。治疗导致生长和骨成熟速度下降,但生长速度也受到性腺外激素(肾上腺)、营养和遗传因素的影响,身高的预测也应小心方法的不准确性,所以成年身高的增加不是GnRHa治疗的全部目的。青春期发身进展速度、取决于个人敏感性的心理学问题、线性生长损失数年的7岁以下开始年龄似乎是决定受累ICPP女孩以GnRHa治疗的主要因素。此外,我们的经验提示,不能确定固定的停止治疗的尺度(BA,CA,身高速度减慢)最好是考虑每个人对身高的满意程度、顺从性和生活质量,包括与其同伴同时出现性征发育。总之,对ICPP的GnRH治疗是安全的,对生殖系统、BMD和BMI的影响是可逆的。对于生长,有助于达到接近TH的AH,但个体反应的可变性提示应当选择除身高增长之外的其它参数,特别是在8岁以上开始青春期发身的女孩。
【金骨龄】专业骨龄及生长发育研究机构,中国骨龄行业标准制定者张绍岩教授任首席科学家,致力于提供适合中国当代少年儿童的骨龄评价技术和生长发育评价服务,独立研发了适用于医疗、体育、司法及母婴行业的骨龄软件 !
【热门文章推荐】

